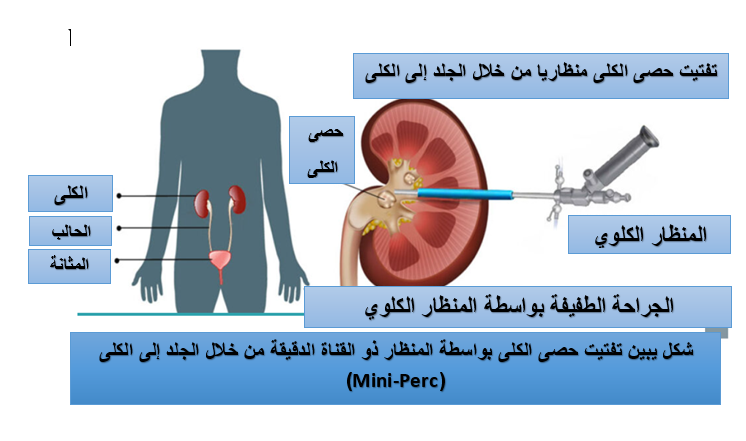
تفتيت حصى الكلى بواسطة المنظار الدقيق (Mini-Perc) وجهاز الـ Trilogy
تفتيت حصى الكلى بواسطة المنظار الدقيق (Mini-Perc) وجهاز الـ Trilogy البروفيسور الدكتور سمير أحمد السامرائي تتكون حصى الكلى من جراء إضطرابات في التوازن بين الترسبات والذوبان للأملاح المتواجدة في البول وخاصة لجميع الحصى التي تحتوي على معدن الكالسيوم [1]. يتأثر حوالي 10% من الأشخاص بالإصابة بحصى الكلى أثناء فترة حياتهم حيث يعاني ما يقارب 70% من الأشخاص المصابون بحصى الكلى من تكرار الإصابة [2]، وفي آسيا يعاني بين 1% إلى 19.1% من الأشخاص هناك بالإصابة بحصى الكلى، ويكون معدل تكرار الإصابة بالحصى هناك بين 21% إلى 53% خلال 3-5 سنوات. في دراسة أجراها Kruck وآخرون، وجدوا بأن معدلات تكرار الإصابة بحصى الكلى كانت أقل بكثير بعد علاجها بواسطة التقنية المنظارية الدقيقة Mini-Perc من خلال الجلد والإستعانة بجهاز تفتيت وشفط الحصى ذو الكفاءة الثلاثية التفتيتية والشفطية والتنقوية والمسمى بجهاز ال (Trilogy) مقارنة بالجراحة المنظارية لحصى الكلى من خلال الحالب (RIRS) [3]. ومن الجدير بالذكر فإن لتجنب حدوث تكرار الإصابة بحصى الكلى وللحفاظ على وظائف الكلى فإنه من الضروري أن تعالج في نفس الوقت جميع الأمراض الأيضية وكذلك التشوهات الخلقية في المسالك البولية قبل البدأ بالعلاج المذكور آنفا [4،5]، أما العلاج الجراحي الحديث فإنه قد تحول من الجراحة المفتوحة لحصى الكلى إلى الجراحة المنظارية [6]، حيث جعل تطور هذا العلاج الحديث بالمنظار ذو القناة الدقيقة من الجلد إلى الكلى (Mini-Perc) هو الأفضل مقارنة بالعلاجات الأخرى، لأن العلاج هذا بالمنظار ذو القناة الدقيقة من الجلد إلى الكلى (Mini-Perc) هو إجراء غير جراحي لتفتيت حصى الكلى التي لا يزيد حجمها على عشرون ملم. في عام 1976، قام Fernstorm و Johanssen بالإبلاغ ولأول مرة عن تفتيت حصى الكلى من خلال فتحة جانبية في الكلية المصابة (PCNL) [7]. ووجد عالميا بأن تفتيت حصى الكلى بواسطة ال (Mini-Perc) هو المفضل بسبب سلامته ونسبة نجاحه الكبيرة وقلة مضاعفاته وإن هذه الجراحة البسيطة ذو القناة الجلدية الدقيقة مستحسنة في جميع الأعمار بما في ذلك لدى الأطفال [8،9]. تتيح هذه الجراحة المنظارية الدقيقة الوصول المباشر إلى الحصى في الكلية المصابة مع قلة في ضرر الأنسجة الكلوية المحيطة بالمنظار الدقيق هذا، كما وأظهرت في الآونة الأخيرة بأن هذه التطورات الجراحية المنظارية الدقيقة من خلال الجلد إلى الكلى (Mini-Perc) بأن هذه التقنية أدت إلى التفتيت والتنقية العالية لهذه الحصى وذلك بالإستعانة بإستخدام الجهاز التفتيتي الحديث الترايلوجي (Trilogy) ذو الكفاءة الثلاثية العالية في التفتيت والتنقية للحصى الكلوية بطريقة (Mini-Perc) المنظارية مع السيطرة على ضغط واطئ داخل الكلية أثناء التفتيت، مع العلم فإن القناة الدقيقة للمنظار الدقيق يتم توسيعها بخطوة واحدة بدلا من التوسيع المتعدد للقناة عند إجراء العملية الكلاسيكية (PCNL) حيث أدت هذه الطريقة الحديثة والدقيقة إلى تراجع واضح في مضاعفات عمليات تفتيت الحصى من خلال الجلد إلى الكلى مقارنة بنتائج العمليات المنظارية الجلدية الكلاسيكية (PCNL) [10]، علاوة على ذلك فإنه أصبح ممكنا بعد الإنتهاء من تفتيت حصى الكلى بواسطة جهاز الترايلوجي (Trilogy) وبطريقة ال Mini-Perc المنظارية الإستغناء عن القسطرة الخارجية في القناة الجلدية وذلك لصغر هذه القناة وإغلاقها السريع بطريقة بسيطة والذي كان غير ممكنا الإستغناء عن القسطرة سابقا بعد إجراء الجراحات المنظارية الجلدية الكلوية الكلاسيكية ذو القناة الواسعة (PCNL) [11،12]. لقد تم الترويج لهذا العلاج (Mini-Perc) الجلدي الكلوي الدقيق باعتباره أيضا علاجًا بديلًا للحصى المتعددة في الحوض الكلوي أو في الكؤوس الكلوية [13]. رغم ذلك فإن خبرة الأخصائي في ذلك تلعب دورًا حاسمًا في نجاح هذه الجراحات المنظارية الدقيقة. الدراسات الإكلينيكية الحديثة تدل على أن إستعمال الثقب ذو القناة الواحدة في الكأس الكلوي السفلي والخلفي لتفتيت هذه الحصى الكلوية هو الأكثر إستخداما وبنسبة 70%، بينما إستخدام الثقب في الكأس المتوسط كانت نسبته 20% وإستخدام ثقب في الكأس العلوي كانت نسبته 10% [14]، الدراسة الإكلينيكية لDesai أكدت بأن إستخدام ثقب قناة في الكأس الكلوي الأعلى لإجراء ال Mini-Perc و فوق الضلع الحادي عشر يكون أكثر أمانًا من المضاعفات للحصى المتواجدة في الكأس الأعلى وكذلك بدون الحاجة إلى وضع قسطرة خارجية للكلية من خلال هذه القناة [15]. لا تزال الدواعي الإكلينيكية لجراحة الثقب ذو القناة الواحدة والصغيرة Mini-Perc هي الإصابة بحصى الكلى مافوق 20 ملم أو الإصابة بعدة حصوات في الكلى مافوق 10 ملم في الكؤوس الأخرى وهذه هي الخيار المفضل والخط الأول في علاج حصى الكلى ليس فقط للتي يتجاوز حجمها 20 مم وإنما للحصوات المذكورة آنفا أيضا، وكما توصى به كل من الجمعية الأوروبية وكذلك الأمريكية لأمراض المسالك البولية [16,17]. كافة التطورات التكنولوجية الأكثر أهمية في مجال التفتيت الداخلي لحصى الكلى إعتمدت حاليا في نجاحها على قابلية و كفاءة الجهاز المفتت للحصى والمسمى بجهاز ال Trilogyوهو أحدث ابتكار في التفتيت الداخلي لحصى الكلى، حيث يعمل هذا الجهاز بقدرة وكفاءة ثلاثية من خلال مسبار واحد ودقيق القطر وبتوليد طاقتين احدها طاقة الموجات التصادمية فوق الصوتية والأخرى طاقة الموجات التصادمية الكهرومغناطيسية ويعمل كذلك بتفريغ باليستي لهذه الطاقة لتفتيت الحصى بدقة وتقنية عالية بالإضافة إلى الشفط المستمر للحصى المفتت وبسرعة فائقة مع تطهير كامل للكلى منها وبتقنية عالية جدا. وقد تم الإبلاغ عن كفاءة هذا الجهاز العالية في التفتيت بناءً على مساحة سطح الحصوة وحجم الحصوة الثلاثي الأبعاد [18,19]، وكما أظهرت بيانات الفحص الوطني البريطاني للـ PCNL [20] بأن نسبة التنقية من الحصى بعد تفتيتها بتقنية ال Mini-Perc وفي نفس الوقت الإستعانة بتفتيتها بالجهاز ذو الكفاءة الثلاثية الترايلوجي ومراقبتها أثناء وبعد التفتيت بواسطة الأشعة السينية وصلت إلى 85٪، وكذلك أظهرت دراسة جهاز الترايلوجي (Trilogy) من قبل الباحث Sabnis وآخرون [19] بأن نسبة التنقية للحصى بعد تفتيتها وتنقيتها بواسطة هذا الجهاز ذو الكفاءة الثلاثية كانت عالية بشكل كبير وبلغت 93٪، والتي قد أثبتت من خلال التصوير التشخيصي بالأشعة السينية أثناء إجراء التفتيت وبعده. على الرغم من أن كفاءة تفتيت الحصى باستخدام جهاز الترايلوجي (Trilogy) يبدو أنها أعلى من تلك الأجهزة المستخدمة بشكل شائع، فإن التباينات في تصفية الحصى يمكن أن يكون بسبب استخدام صيغ مختلفة لحساب مساحة سطح الحصى وحجمه الثلاثي الأبعاد. <br>ومن المعروف بأن الصيغة التقليدية لمعرفة حجم الحصى قد تقدر حجم الحصى ثلاثي الأبعاد بطريقة مفرطة أو غير كافية بالمقارنة مع القياسات المحوسبة بواسطة الأشعة السينية المقطعية [21]. كما وأظهرت دراسة لخودير وآخرين دليلاً على سلامة الأنسجة عند استخدام الجهاز ذو الكفاءة الثلاثية ال [22] Trilogy ، وكما أضهرت هذه الدراسة بأنه لم تحدث أي مضاعفات كبرى درجةClavien IV-V) ) ولكن كان معدل المضاعفات العامة 9.5٪، ومعدل نقل الدم 2٪. التقنية المصغرة الجراحية (MINI-PERC) هي تقنية فعالة وآمنة لعلاج الحصوات الكلوية المتوسطة الحجم، وتمثل حل وسط معقول بين تقنية ال MINI-PERC القياسية والمنظار الحالبي والكلوي الداخلي (RIRS) المرن وإننا نؤكد بمراجعتنا للدراسات
تفتيت حصى الكلى بواسطة المنظار الدقيق (Mini-Perc) وجهاز الـ Trilogy قراءة المزيد »