هل يمكن للتشخيص وللإستئصال الجذري المبكر لسرطان البروستاتا أن يتنبأ بنتائج شفاء منه وعدم إنتشاره موضعيا؟
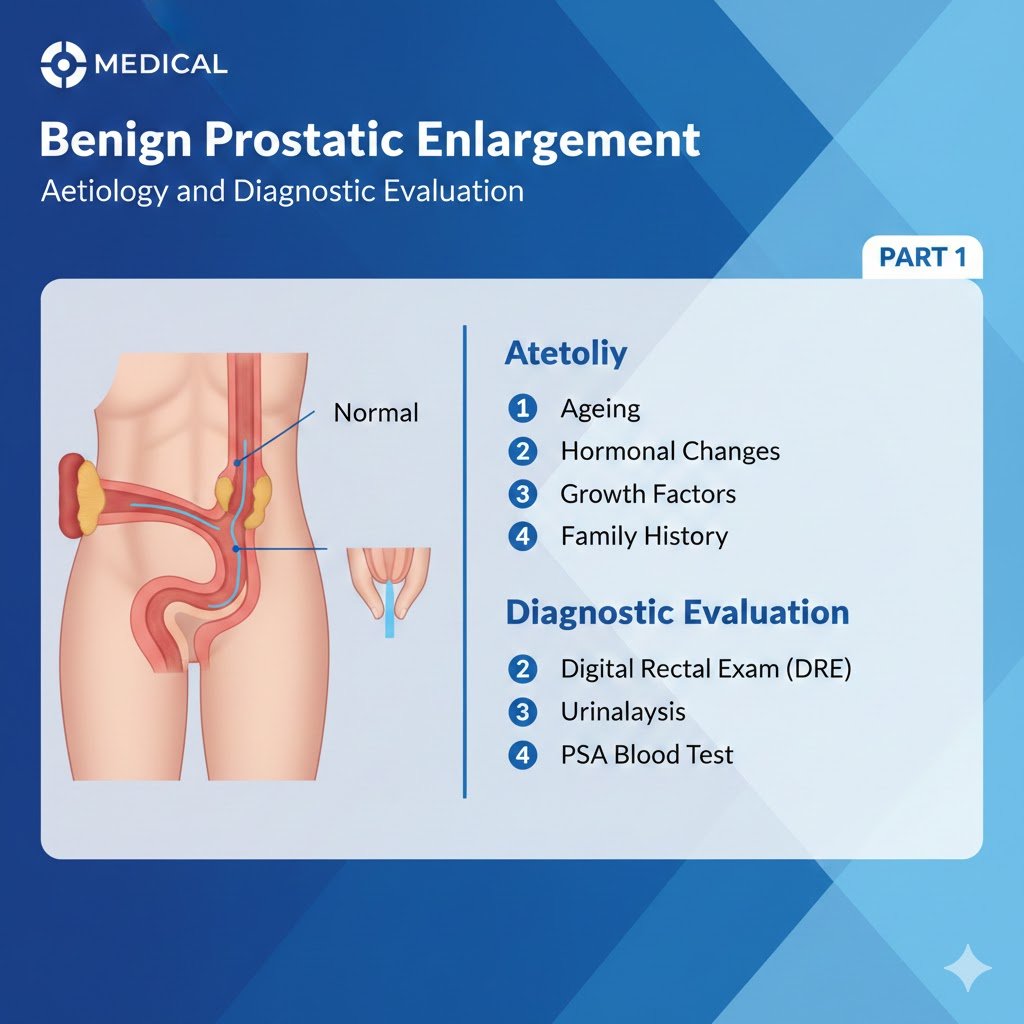
هل يمكن للتشخيص وللإستئصال الجذري المبكر لسرطان البروستاتا أن يتنبأ بنتائج شفاء منه وعدم إنتشاره موضعيا؟ البروفيسور الدكتور سمير أحمد السامرائي نعم يمكن التنبأ بنتائج الشفاء من سرطان البروستاتا إذا أعتمد على التشخيص الحديث ذو الخصوصية والحساسية العالية كالكشف المبكر من خلال اختبار المستضد البروستاتي النوعي في الدم وكذلك تشخيص كثافة ال PSA المسمى (PSAD) ومن ثم الخزعة البروستاتية المعتمدة على الإندماج الموجه من خلال التصوير الديناميكي لصور الرنين المغناطيسي وصور البروستاتا مع التصوير بالموجات فوق الصوتية عن طريق المستقيم لتجرى الخزعة البروستاتية بتقنية وبنسبة عالية للحصول على الخلايا أو التغيرات التي أكتشفت من خلال تصوير الرنين المغناطيسي ودمجها مع تصوير الموجات فوق الصوتية لغدة البروستاتا أثناء أخذ الخزعة وتحت التخدير الموضعي، وكذلك إذا أعتمد على العلاج الروبوتي الحديث بواسطة الروبوت DAVINCI XI الذي يقوم بإجراء جراحة طفيفة التوغل مع تشخيص الحافة الجراحية الإيجابية (PSMs) أثناء إستئصال البروستاتا الجذري بواسطة الروبوت DaVinci XI بواسطة إستعمال الدليل الواقعي الإضافي والمعززوالموجه المعرفي بواسطة تصوير الرنين المغناطيسي المتعدد المعالم (mp MRI) والذي يسهل أخذ الخزعة المقطعية المجمدة أثناء ذلك وبدون التأثير على السلامة الأنكولوجية فيها مخفضة خطورة عدم إكتشاف الحواف الإيجابية أثناء هذه الجراحة. يعد سرطان البروستاتا (PCa) مصدر قلق صحي كبير في جميع أنحاء العالم حيث يعاني ما يصل إلى 60٪ من المرضى من انتكاس كيميائي حيوي بعد العلاج الجذري لسرطان البروستاتا، ويعتبر ثاني وأكثر أنواع السرطانات شيوعًا لدى الذكور والسبب الخامس لوفيات السرطان لديهم في جميع أنحاء العالم [1]، وتشخص إصابة بهذا السرطان بنسبة 13-17% خلال فترة حياتهم ولرجل واحد من كل ستة إلى ثمانية رجال، وفي أوروبا تم الإبلاغ حديثا عن 340.000 إصابة جديدة و70.000 حالة وفاة سنويا مرتبطة بسرطان البروستاتا. سبب الإصابة به تعزى من قبل الوكالة الدولية لبحوث السرطان إلى نمو السكان عالميا، إرتفاع نسبة الشيخوخة عالميا وتقدم العمر كذلك مسؤول بنسبة عالية على الإصابة بهذا السرطان، أما التوارث العائلي والخلفية العرقية وكما أثبتته عدة دراسات إكلينيكية فإنه المسؤول الرئيسي لإرتفاع الإصابة بسرطان البروستاتا في عمر مبكر وخاصة لدى هؤلاء الذين لديهم إستعداد جيني لذلك [2,3]، وتكون نتيجة طفرات جينية وراثية في الجين (ه.ب.س.ل) في الذراع القصير للكروموزوم (واي) مؤديا إلى الإصابة بهذا السرطان مبكرا أي ب 6-7 سنوات [4]. وكما وأكدت الدراسات الحديثة بأن طفرات جينات أخرى وخاصة ال (ب.ر.ك.أ-2) و (ب.ر.ك.أ-1) وهذه أكدت بأنها عوامل خطورة وراثية مهيئة للإصابة بهذا السرطان [2,5]. وكما أثبتت الدراسات الإكلينيكية العالمية بأن إرتفاع المخاطر بالإصابة بهذا السرطان البروستاتي الوراثي كان الأعلى من مخاطر الإصابة بتلك السرطانات العائلية الأخرى كسرطان الثدي وسرطان المبيض الوراثي وسرطان القولون والمستقيم الوراثيين. أما إحتمال الإصابة بسرطان البروستاتا ذو الخطورة السرطانية العالية فإن نسبته قد بلغت 11% في سن ال 65 من العمر، خطورة تردء مراحل هذا السرطان و مقاومته الهرمونية تكمن في إصابة واحد من كل خمسة رجال يتم تشخيص السرطان عندهم. دراسة إكلينيكية حديثة أثبتت بعد متابعة رجال إكلينيكيا وسريريا سنويا و لمدة ثلاث سنوات ما بين سن ال 40-69، مع أخذ خزعة من غدة البروستاتا وقياس مستوى ال PSA والذي كان مافوق 3نانوغرام/مل والذين توجد لديهم مخاطر بالإصابة بسرطان البروستاتا الوراثي جينيا وخاصة بسبب طفرات في سلالة الجين (ب.ر.ك.أ 2) أنه بعد 3 سنوات من هذه الفحوصات التشخيصية السريرية شخص لديهم إرتفاع في معدل الإصابة بهذا السرطان رغم صغر سنهم أثناء التشخيص [6]. أما الدراسات الإحصائية الخاصة بالإصابة بسرطان البروستاتا من جراء التغير البيئي الخارجي (الهوائي والمائي والغذائي) فإنها دلت على أنها عوامل الخطورة المؤدية أيضا إلى الإصابة بنسبة عالية بهذا السرطان مسببة تطوره من سرطان كامن إلى سرطان سريري [7]. وكذلك دلت هذه الدراسات على أن الإصابة بالمتلازمة الأيضية وخاصة السمنة وإرتفاع محيط الخصر إلى مافوق 102 سم و الإصابة بإرتفاع ضغط الدم لها علاقة وطيدة بإرتفاع خطورة أكبر بالإصابة بسرطان البروستاتا، وفي نفس الوقت وخاصة إزدياد الإصابة بالسرطان ذو الدرجة العالية لدى الرجال المصابون بالسمنة المفرطة [8]. أما عوامل الخطورة المحتملة الأخرى للإصابة بسرطان البروستاتا فإنها تكون نسبة الإصابة مرتفعة عند هؤلاء الرجال الذين يصابون بمرض التهاب الأمعاء مقارنة مع عامة السكان [9]، وكذلك الإصابة بالجرثوم الإحليلي السيلاني أدى إلى إرتفاع إصابة هؤلاء بسرطان البروستاتا [10]. أما إرتباط التدخين في تكون هذا السرطان فإنه يؤدي أيضا إلى زيادة خطر الموت بسبب الإصابة بهذا السرطان [11،12]. أما الرجال الذين يصابون بفيروس الورم الحليمي البشري (HPV-16) فإنهم قد يكونون في خطر متزايد بالإصابة بسرطان البروستاتا [12]. أما وجود تركيز مرتفع النسبة من المبيد الحشري الكلورديكون الأستروجيني في الدم فإنه يؤدي إلى إرتفاع خطر الإصابة بسرطان البروستاتا [13]. أما أعراض الإصابة بسرطان البروستاتا فإنها تكون لها علاقة بتغيرات مرضية تفريغية وتضيقية في الإحليل وعنق المثانة مؤدية إلى ضعف التيار التدفقي أثناء التبول وتغيرات تخزينية مؤدية إلى التبول الإلحاحي والسلس الإلحاحي والتردد ليلا ونهارا للتبول. تسبق الإصابة بإنتشار سرطان البروستاتا في الجسم عودة إرتفاع مستوى المستضد النوعي في دم المصاب بهذا السرطان أثناء فترة من الزمن مابين 7 إلى 8 سنوات بعد الإستئصال الجذري أو العلاج الإشعاعي لهذا السرطان، وعندما يُشتبه في حدوث انتكاس كيميائي حيوي (Biochemical relapse) ويتجاوز مستوى المستضد النوعي البروستاتي (PSA) إلى مافوق 0.2 نانوغرام / مل فإن الحاجة تصبح ملحة للجوء إلى الأجهزة التصويرية البوزيترونية (PET)، حيث دلت الدراسات الإكلينيكية لأجهزة التتبع الإشعاعية (Radiotracer) والتي تستهدف مؤشرات في خلايا سرطان البروستاتا بأن إستخدام غشاء المستضد النوعي البروستاتي في التصوير (PSMA) حضى الآن بأكبر قدر من الإهتمام في هذا المجال التشخيصي المهم وفي تشخيص التكرار الكيميائي الحيوي لسرطان البروستاتا بعد الإستئصال الجذري لهذا السرطان فإن التطبيق الأكثر دراسة إكلينيكيا وعلى نطاق واسع كان للتصوير بواسطة ال PSMA حيث تم الإبلاغ من خلال أكبر دراستين إكلينيكيتين بتأكيد تقييم النتائج التشخيصية الإيجابية بواسطة التصوير(68Ga-PSMA PET / CT) بنسبة 82% وخاصة للذين أشتبه بإصابتهم في تكرار السرطان بعد الإستئصال الجذري له وكذلك بعد علاجهم بالحرمان الهرموني ADT [14] حيث ارتبط معدل التشخيص عن الإنتشار بشكل طردي مع إرتفاع مستوى ال PSA في دم المصاب وخاصة عند إرتفاع هذا المستوى إلى مافوق 20 نانوغرام/مل وفي نفس الوقت أدى هذا الإرتفاع لمستوى ال PSA إلى تحسن الحساسية التشخيصية لهذه الطريقة التصويرية الحديثة بنسبة 100%، بينما دلت دراسة أخرى [15] إلى إكتشاف النشوء السرطاني بنسبة 60% عندما كان مستوى ال PSA تحت 2.2 نانوغرام/مل وكان الإكتشاف لنشوء سرطاني بروستاتي بنسبة 100% عندما كان مستوى ال PSA مافوق 2.2 نانوغرام/مل. عند اكتشافه مبكرًا، وخاصة في حالة إكتشاف الإصابة بالسرطان بمرحلة مبكرة وموضعية في غدة البروستاتا وإستئصاله جذريا، فإن فترة البقاء على قيد الحياة تكون بنسبة 100% لمدة 5